"Čudesni" lek dobio zeleno svetlo: Da li dozvola za lekanemab znači "početak kraja" Alchajmerove bolesti?
Komentari
23/08/2024
-09:15
Prvi lek za koji je utvrđeno da usporava Alchajmerovu bolest trebalo bi da dobije zeleno svetlo za upotrebu u Britaniji.
Utvrđeno je da lekanemab, koji su stručnjaci pozdravili kao "početak kraja" bolesti, usporava kognitivni pad kod obolelih za - 27 odsto.
Očekuje se da će u četvrtak Regulatorna agencija za lekove i zdravstvene proizvode (MHRA) dati odobrenje za lečenje rane Alchajmerove bolesti.
Ova odluka organa za bezbednost lekova značiće da se prvi put može privatno prepisati, barem u Britaniji.
Nacionalni institut za zdravlje i brigu će zatim savetovati da li bi ga trebalo da uvede NHS (National Health Service).
Lek, koji se daje svake dve nedelje intravenski, prvi je tretman koji modifikuje bolest kako bi usporio kognitivni pad i smanjio plakove povezane sa bolešću.
Klinička ispitivanja su pokazala da je usporio pad pamćenja i funkcionalnog razmišljanja učesnika.
Lečenje je prošle godine odobrila američka Uprava za hranu i lekove.
Rizik od neželjenih efekata
Međutim, Evropska agencija za lekove bila je daleko opreznija. Prošlog meseca je odbila licencu za lek, rekavši da su potencijalni neželjeni efekti, uključujući "otok i potencijalna krvarenja u mozgu", veći od uticaja koji je imao na usporavanje napredovanja Alchajmerove bolesti, piše BBC.
Očekuje se da će MHRA postaviti neka obavezujuća pravila kako bi se smanjio rizik od neželjenih efekata kada odobri lekanemab.
Ona uključuju pacijente sa APOE genom, koji nosi oko četvrtine ljudi. Utvrđeno je da oni sa APOE genom, koji povećava rizik od Alchajmerove bolesti, imaju veći rizik od amiloidnih abnormalnosti (Aria), koje karakterišu oticanje i krvarenje mozga.
Unsplash

Pacijenti koji uzimaju neke vrste lekova za razređivanje krvi takođe će biti isključeni zbog povećanog rizika od krvarenja.
Portparol MHRA je rekao:
"Trenutno završavamo rigoroznu procenu dokaza koji podržavaju lekanemab u lečenju Alchajmerove bolesti. Dodatne informacije biće blagovremeno saopštene".
Napravili - Japanci
Dok su obimna ispitivanja pokazala da lekanemab, koji proizvodi Eisai, japanska farmaceutska kompanija, usporava rane faze Alchajmerove bolesti, njegova efikasnost zavisi od rane dijagnoze, korišćenjem specijalističkih skeniranja i istraživanja.
Rezultati ispitivanja prošle godine bili su prvi pozitivni pomaci u lečenju za skoro tri decenije, što sugeriše da lekanemab usporava napredovanje bolesti, a ne samo maskira simptome.
Ali tretman zahteva daleko više dijagnostičkih kapaciteta, sa MRI skeniranjem, lumbalnim punkcijama i PET skeniranjem potrebnim da bi se utvrdilo koji slučajevi će imati koristi od lekova.
Lekanemab je dizajniran da cilja i očisti amiloid, jedan od proteina koji se nakuplja u mozgu ljudi sa Alchajmerovom bolešću u ranoj fazi bolesti.
Tanjug AP Charles Krupa Matt York EPA David A. White BIOGEN.jpg
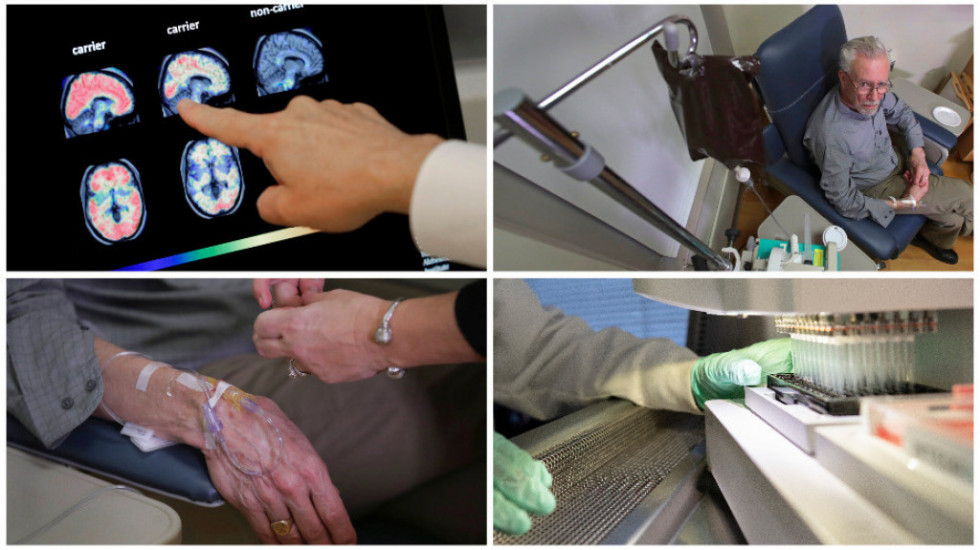
Studija, nazvana Clarity AD, bila je najveća do sada koja je testirala teoriju o kojoj se dugo raspravljalo da bi čišćenje amiloidnih toksičnih moždanih plakova moglo da uspori napredak Alchajmerove bolesti.
Naučnici su uporedili rezultate ljudi koji su uzimali lek sa onima koji su uzimali placebo - ili lažni lek. Posle 18 meseci, otkriveno je da je lek usporio napredovanje bolesti za 27 odsto.
Ispitivanja su pokazala razlike u nakupljanju amiloida u mozgu u skeniranju učesnika, pri čemu su oni koji su uzimali lek imali niže nivoe od onih koji su uzimali placebo.
Studija je otkrila da su najčešći neželjeni efekti bili glavobolja i otok Aria.
Uvođenje u državne ustanove zahteva prošireni dijagnostički kapacitet
U januaru 2023. godine, lekanemab je odobren za upotrebu u Sjedinjenim Državama, koristeći proces "ubrzanog odobrenja" po ceni od 26.500 dolara godišnje.
Uvođenje u NHS bi zahtevalo masovno proširenje dijagnostičkih kapaciteta, kako bi se utvrdilo ko bi mogao imati koristi, i zahtevalo bi široku upotrebu genskih testova.
Revizija objavljena ranije ovog meseca pokazala je da samo 2,1 odsto ljudi sa demencijom prolazi kroz sve specijalističke pretrage koje su potrebne.
Najvažnija je rana dijagnoza
Stručnjaci su takođe rekli da efikasnost takvih tretmana zavisi od rane dijagnoze.
Program National Audit of Dementia je takođe utvrdio da je prosečno vreme čekanja od upućivanja na pregled do dijagnoze dostiglo pet meseci.
Prema Alzheimer’s Society, oko 982.000 ljudi u Velikoj Britaniji živi sa demencijom. Očekuje se da će ta cifra dostići 1,4 miliona do 2040. godine.
Profesor Džon Hardi, jedan od vodećih svetskih istraživača u ovoj oblasti, rekao je da lek "menja igru", opisujući ga kao "najveći proboj u Alchajmeru decenijama".
Profesor Hardi, predsednik odeljenja za molekularnu biologiju neuroloških bolesti na UCL Institutu za neurologiju, rekao je:
Unsplash
"Nema sumnje da je ovo najveći napredak u poslednjih 30 godina".
Kada su rezultati ispitivanja objavljeni u novembru 2022., opisao je lekanemab kao "početak kraja" za Alchajmerovu bolest.
"To usporava bolest. Usporava je za oko 25 do 30 odsto", rekao je on.
"Dakle, znate, možda, ako ste u ranije dobili pet godina pre nego što odete u starački dom, sada biste mogli dobiti sedam godina pre nego što završite u staračkom domu".
Britanska organizacija Alzheimer’s Research saopštila je da su ova otkrića "istorijski trenutak" u istraživanju demencije.























Komentari (0)